简介
氢化硅烷是一类相对稳定的化合物,但在是金属催化剂存在的条件下,可以与不饱和键发生加成反应。该方法已日益发展成为有机硅化合物的合成方法。近年来,在半导体的表面修饰和一些功能材料的开发中发挥着重要的作用。
[CP*RU(MECN)3]PF6:一种高效的氢化硅催化剂
乙烯基硅烷是多用途有机金属试剂,参与多种反应,例如Tamao–Fleming氧化、烯烃复分解、钯催化交叉偶联、原脱甲硅烷化和环加成。在制备乙烯基硅烷的可用方法中,炔烃的氢化硅烷化是最直接和具有原子经济性的方法(方案1)。同时,已经设计了许多过渡金属催化剂以区域和立体控制的方式执行这些反应(图1)。

方案1.炔烃的氢化硅烷化
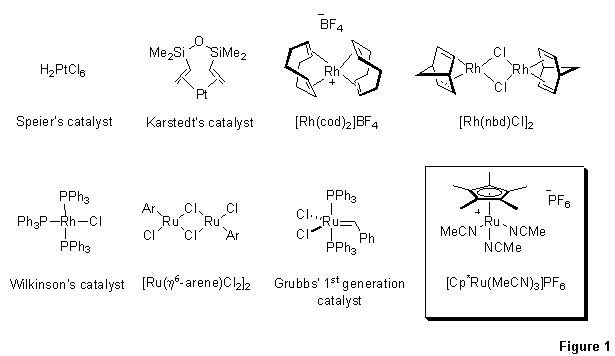
图1.设计了以区域和立体控制的方式进行反应的过渡金属催化剂。
末端炔烃的氢化硅烷化方法是在不久前发展起来的,用于制备顺式和反式β-乙烯基硅烷。经典的铂催化(Speier's和Karstedt's催化剂)1-5以及基于铑的催化([Rh(cod)2]BF4和[RhC(nbd)]2)6-9仍然是合成反式β-乙烯基硅烷的有力方法。Wilkinson催化剂也被验证在极性溶剂中产生反式产物,而在非极性介质中以顺式异构体为主。钌催化剂(例如[Ru(benzene)Cl2或[Ru(p-cymene)Cl2]可得到顺式-β-乙烯基硅烷10-13。尽管氢化硅烷化的立体选择性和区域选择性高度依赖于炔烃、硅烷和溶剂,但在某些条件下,第一代Grubbs催化剂也产生顺式产物。尽管存在大量制备线性β-乙烯基硅烷的方法,但直到最近,还没有制备1,1-双取代α-乙烯基硅烷的通用方法。此外,尽管可以实现内部炔烃分子内部的选择性氢化硅烷化,分子间变体的选择性实际上是未知的。斯坦福大学的Trost课题组开发了一种非常稳健的方案,通过[CP*RU(MECN)3]PF6实现末端乙炔的氢化硅烷化以得到α-乙烯基硅烷14。该催化剂还为内部炔烃的区域选择性分子内和分子间氢化硅烷化提供了一种仅生成Z-三取代烯烃的有效方法。
分子间氢化硅烷化:末端炔烃类
在[Cp*Ru(MeCN)3]PF6的存在下,一组不同的末端炔烃进行快速和温和的氢化硅烷化,以良好到优异的产率和低催化剂负载量得到1,1-双取代α-乙烯基硅烷(方案2)。该反应能耐受多种官能团,包括卤素、游离醇、烯烃、内炔烃、酯和胺。此外,可以在具有良好的可预测性反应中使用大量硅烷。

方案2.分子间氢化硅烷化:末端炔烃
分子间氢化硅烷化:内部炔烃类
如方案1所示,内炔烃的非选择性氢化硅烷化将可能产生四种异构体加成产物。Trost课题组已经证明,内炔烃与[Cp*Ru(MeCN)3]PF6的氢化硅烷化仅产生三取代的Z-乙烯基硅烷,这是硅烷向炔烃反加成结果(方案3)15。
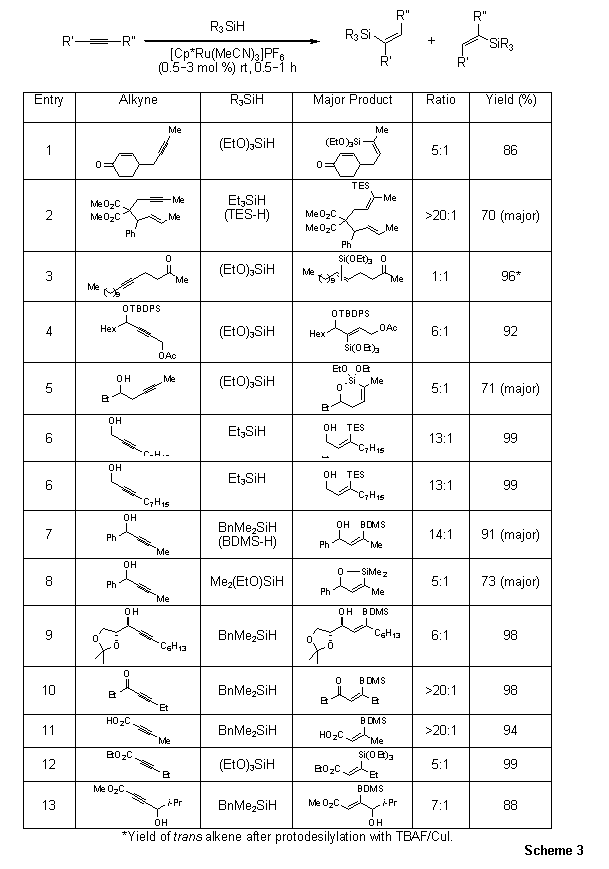
方案3.分子间氢甲硅烷化:内部炔烃
重要的是,氢化硅烷化反应表现出了高水平的区域选择性。区域选择性可概括如下:(i)2-炔烃的氢化硅烷化导致Z-烯烃的形成,其中硅烷基占据空间要求较低的位置(1&2);(ii)对于炔烃不在2-位的底物,硅烷取代基将占据空间要求较高的位置(4);(iii)对于炔丙基、高炔丙基和高炔丙醇底物,发生氢化硅烷化,使得硅烷基位于Z-烯烃的羟基官能团的远端(5-9);(iv)在α,β-炔基羰基的情况下,硅烷基再次选择性地占据Z-烯烃的远端位置(10–13)15,16。对于游离炔丙基、高炔丙基和高炔丙醇底物,与带有离去基团(例如乙氧基取代基)的硅烷氢化硅烷化形成环状硅氧烷(5&8)。值得注意的是,使用[Cp*Ru(MeCN)3]PF6的氢化硅烷化可以在保持炔基中不对称中心的立体化学完整性的同时进行(9)。最后,尽管非空间分化的炔烃经历立体但非区域选择性的氢化硅烷化(3),但产物混合物的原脱硅提供了单一的反式非对映体。这对在Lindlar还原条件下观察到的顺式选择性提供了有价值的补充。
如方案4所示,即使是高活性硅烷也可以以优异的可预测性参与分子间氢化硅烷化反应。生成的烯基氯硅烷与己二烯醇结合,生成硅氧烷键。加热三烯导致分子内Diels-Alder(IMDA)反应,生成具有四个连续立体中心的硅氧烷。然后可以将加合物进行原脱硅或Tamao–Fleming条件处理以分别提供伯醇或二醇。

方案4. 高活性硅烷可以以优异的可预测性参与分子间氢化硅烷化反应。
在原脱硅或氧化之前处理烯烃也是可行的。例如,乙烯基硅烷容易被m-CPBA以非对映选择性方式环氧化(方案5)。随后的原脱硅提供了相应的合成环氧醇,而Tamao–Fleming氧化提供了合成二醇。因此,这个过程可以作为羟醛缩合的替代物。
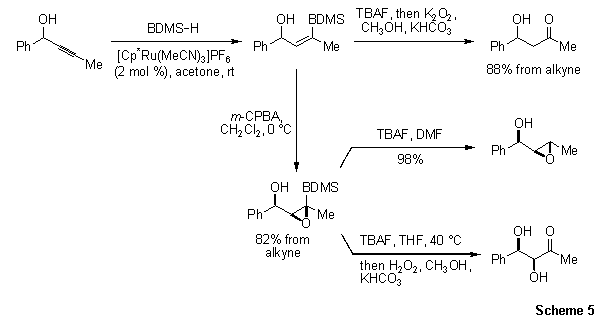
方案5.乙烯基硅烷容易被m-CPBA以非对映选择性方式环氧化。
分子内部氢化硅烷化
最后,使用羟基炔烃可以实现分子内氢化硅烷化,如方案6所示的3-hydroxypiperidine alkaloid (+)-spectaline合成方案17。用四甲基二硅氮烷(TMDS)处理高炔丙醇,然后进行区域(远端)和立体选择性(Z)分子内氢化硅烷化,得到环状叠氮硅氧烷。通过Tamao–Fleming氧化,然后还原并伴随环化,以可观的产率得到该产物。
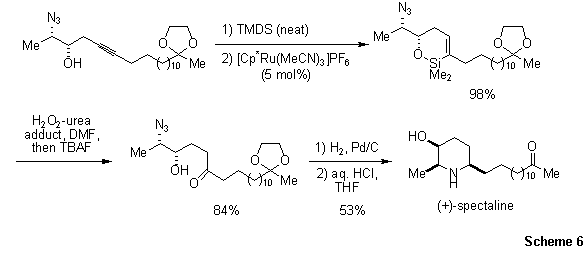
方案6. 3-hydroxypiperidine alkaloid (+)-spectaline的合成
分子内氢化硅烷化和随后的交叉偶联为在游离羟基位于远端的炔碳上引入新的碳键提供了一种极好的方法(方案7)18。
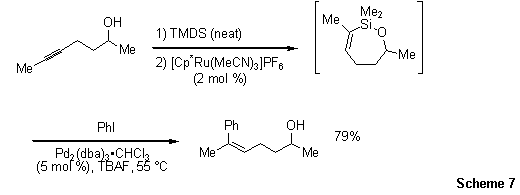
方案7.游离羟基位于远端的炔碳
阿拉丁为您提供[Cp*Ru(MeCN)3]PF6,以及其他多种氢化硅烷化催化剂。
参考文献
1. Speier, J. L.; Webster, J. A.; Bernes, G. H. J. Am. Chem. Soc. 1957, 79, 974. https://doi.org/10.1021/ja01561a054
2. Lewis, L. N.; Sy, K. G. ; Bryant, G. L.; Donahue, P. E. Organometallics 1991, 10, 3750. https://doi.org/10.1021/om00056a055
3. Denmark, S. E; Wang, Z. Org. Lett. 2001, 3, 1073. https://doi.org/10.1021/ol0156751
4. Itami, K.; Mitsudo, K.; Nishino, A.; Yoshida, J. J. Org. Chem. 2002, 67, 2645. https://doi.org/10.1021/jo0163389
5. Kettler, P. B. Org. Proc. Res. Dev. 2003, 7, 342. https://doi.org/10.1021/op034017o
6. Ojima, I.; Kumagai, M. J. Organomet. Chem. 1974, 66, C14. https://doi.org/10.1016/S0022-328X(00)93873-7
7. Dickers, H. M.; Haszeldine, R. N.; Mather, A. P.; Parish, R. V. J. Organomet. Chem. 1978, 161, 91. https://doi.org/10.1016/S0022-328X(00)80914-6
8. Takeuchi, R.; Tanouchi, N. J. Chem. Soc., Perkin Trans. 1 1994, 2909. https://doi.org/10.1039/P19940002909
9. Takeuchi, R.; Nitta, S.; Watanabe, D. J. Org. Chem. 1995, 60, 3045. https://doi.org/10.1021/jo00115a020
10. Esteruelas, M. A.; Herrero, J.; Oro, L. A. Organometallics 1993, 12, 2377. https://doi.org/10.1021/om00030a057
11. Na, Y.; Chang, S. Org. Lett. 2000, 2, 1887. https://doi.org/10.1021/ol0059697
12. Trost, B. M.; Ball, Z. T. J. Am. Chem. Soc. 2001, 123, 12726. https://doi.org/10.1021/ja0121033
13.Trost, B. M.; Ball, Z. T. J. Am. Chem. Soc. 2005, 127, 17644. https://doi.org/10.1021/ja0528580
14. Trost Barry M.,Ball Zachary T.. Intramolecular Endo-Dig Hydrosilylation Catalyzed by Ruthenium: Evidence for a New Mechanistic Pathway[J]. J. Am. Chem. Soc.,2002,125(1).
https://doi.org/10.1021/ja028766h
15. Denmark SE, Pan W. 2002. Org. Lett.. 44163.
16. Chung LWea. 2003. J. Am. Chem. Soc.. 12511578.
17. Trost BM, Ball ZT, Jöge T. 2002. A Chemoselective Reduction of Alkynes to (E)-Alkenes. J. Am. Chem. Soc.. 124(27):7922-7923. https://doi.org/10.1021/ja026457l
18. Trost BM, Machacek MR, Ball ZT. 2003. Ruthenium-Catalyzed Vinylsilane Synthesis and Cross-Coupling as a Selective Approach to Alkenes: Benzyldimethylsilyl as a Robust Vinylmetal Functionality. Org. Lett.. 5(11):1895-1898. https://doi.org/10.1021/ol034463w

